Современные подходы к диагностике и лечению аденом гипофиза и других образований хиазмально-селлярной области
Хиазмально-селлярной областью называется анатомическая зона, включающая участок клиновидной кости между передними наклоненными отростками и спинкой турецкого седла. В этой области различают внутренние отверстия зрительных каналов, площадку основной кости с бугорком турецкого седла, предперекрестную борозду, турецкое седло, содержащее гипофиз, спинку турецкого седла. Кверху от указанных образований располагается субарахноидальная цистерна перекреста зрительных нервов, содержащая собственно перекрест, конечные отделы зрительных нервов и начальные отделы зрительных трактов, и ограниченная сзади мембраной Лилиеквиста; над ней располагается воронка гипофиза и сосочковые тела. Снаружи область ограничена цистернами сонных артерий и медиальными стенками кавернозных синусов.
Новообразования хиазмально-селлярной области представлены группой разнородных по происхождению, патогенезу, клиническим проявлениям и биологическим свойствам опухолей. В нашем обзоре они объединены лишь по анатомо-топографическому критерию, который подразумевает возможность общего транссфеноидального эндоскопического хирургического подхода к ним.
Из образований хиазмально-селлярной области выделяют аденомы гипофиза, краниофарингиомы, менингиомы, кисты кармана Ратке, глиомы, арахноидальные кисты, хондромы, хордомы и другие.
Аденомы гипофиза представляют собой разнородную группу опухолей, исходящих из передней доли гипофиза – аденогипофиза, и являются самыми распространенными образованиями хиазмально-селлярной области. Вторыми по частоте встречаемости являются краниофарингиомы. Далее следуют менингиомы бугорка и диафрагмы турецкого седла. Другие новообразования встречаются значительно реже.
Краниофарингиомы – это дизэмбриогенетические опухоли, формирующиеся из кармана Ратке (глоточно-гипофизарный вырост эмбрионального эпителия, идущий от дна III желудочка до задней стенки глотки, участвующий в закладке передней доли гипофиза). Обычно эти новообразования имеют солидную часть, нередко с включением петрификатов, и кистозную часть.
Менингиомы бугорка турецкого седла. Проявляются обычно прогрессирующим снижением зрения. Диагностика и хирургическое лечение этих новообразований не отличается от общих принципов диагностики и лечения менингиом основания черепа.
Опухоли зрительных нервов и зрительного перекреста обычно имеют гистологическую характеристику астроцитом. Как правило, являются доброкачественными опухолями. Чаще являются двусторонними.
Эпидемиология. Аденомы гипофиза занимают третье место по частоте встречаемости среди всех первичных интракраниальных опухолей (после глиом и менингиом), что составляет по данным различных авторов от 7,3% до 18%. Наиболее часто заболевание наблюдается у лиц молодого и трудоспособного возраста: в 75% случаев приходится на возраст от 20 до 50 лет [8,13,11,23,37]. Распространенность гормональноактивных аденом составляет до 20 на 1000000 населения, с ежегодным выявлением 2 случаев на 1000000. Распространенность неактивных аденом гипофиза, по данным различных авторов, до 70-90 случаев на 1000000 [8,37]. В структуре всех аденом гипофиза наиболее часто встречаются пролактиномы и гормональнонеактивные опухоли гипофиза (приблизительно по 35%), СТГ- и АКТГ- продуцирующие опухоли составляют по 10-15% всех аденом, ТТГ- продуцирующая опухоль встречается крайне редко [2,3,8,9]. Соотношение мужчин и женщин в группе неактивных аденом равное. Заболеваемость аденомами гипофиза увеличивается с возрастом.
Краниофарингиомы. Обычно встречаются у детей и подростков; в этой возрастной группе по частоте уступают только медуллобластомам и астроцитомам. У взрослых встречаются редко, но пик заболевания приходится на возрастную группу 50-60 лет [37].
Менингиомы хиазмально-селлярной области встречаются до 9,5% от всех внутричерепных менингиом, и до 3% всех внутричерепных опухолей [10].
Глиомы зрительных нервов. Встречаются почти исключительно в детском и подростковом возрасте.
Другие новообразования хиазмально-селлярной области встречаются значительно реже.
Клиническая картина. Аденомы гипофиза проявляются признаками гормональной дисфункции передней доли гипофиза и/или симптомами, связанными с объемным воздействием массы опухоли на окружающие структуры гипоталамо-гипофизарной области [2,3,8,9,37]. Признаками гормональной дисфункции могут быть избыточная выработка гормонов передней доли гипофиза, либо угнетение секреции питуитарных гормонов в различной степени (от дефицита секреции одного гормона до пангипопитуитаризма). Масс-эффект может быть местным (селлярным), и супраселлярным. Местное объемное воздействие выражается в недостаточности секреции гормонов гипофиза, а супраселлярное - компрессией смежных супраселлярных структур.
Клиническая картина краниофарингиом представлена нарушениями функции гипофиза, гипоталамуса, ствола мозга, включая черепно-мозговые нервы. Гормональная дисфункция (в виде недостаточности одного или нескольких гормонов гипофиза) встречается у 60% пациентов. У взрослых чаще встречается гипогонадизм, у детей – задержка роста и полового созревания. Несахарный диабет встречается, по данным разных авторов, у 15-30% пациентов [3,9,37]. Визуальные нарушения в виде снижения остроты зрения, или нарушения полей зрения встречаются у 50-75%. Общемозговая симптоматика наиболее часто представлена головной болью, и отмечается у 57% пациентов [37].
Клиника менингиом указанной области проявляется нарушением зрения, чаще ассиметричным [10].
Глиомы зрительных нервов проявляются прогрессирующим снижением зрения вплоть до амавроза [6].
Клиническая картина других редко встречающихся опухолей не является специфической, и представлена общемозговыми симптомами, и симптомами локального воздействия опухолей.
Гормональнонеактивные аденомы гипофиза: у 75% всех пациентов имеется недостаточность выработки тропных гормонов гипофиза. Из них гипотиреоидизм встречается у 30%, адреналовая недостаточность у 25% пациентов [39]. Гипогонадизм проявляется снижением либидо, бесплодием, эректильной дисфункцией у мужчин, аменореей и бесплодием у женщин. Гипотиреоидизм проявляется головной болью, депрессией, снижением ментальных функций, увеличением массы тела, запорами. Дефицит гормона роста у взрослых пациентов характеризуется снижением общей сопротивляемости, ожирением, снижением минеральной плотности костей с повышенным риском переломов, тревожностью, беспокойством, частой сменой настроения. АКТГ недостаточность проявляется общей слабостью, утомляемостью, анорексией, миалгией, артралгией, гастроинтестинальным синдромом, ортостатическими проявлениями. В случае остро наступившей декомпенсации надпочечниковой недостаточности (или Аддисонова криза) клиническая картина может проявляться гастроинтестинальным синдромом, головной болью, зрительными нарушениями, гипонатриемией, расстройствами сознания, сердечно – сосудистым коллапсом [23].
Резкая, внезапно наступившая питуитарная недостаточность может быть следствием гипофизарной апоплексии [1]. Для нее характерно острое начало, резкая головная боль, возможно нарушение сознания, зрительные нарушения в виде хиазмального синдрома, снижение остроты зрения вплоть до полной слепоты, клиника гипофизарной недостаточности. Для ее верификации необходимо проведение КТ (МРТ) головного мозга по экстренным показаниям.
Клинические проявления супраселлярного распространения опухоли.
Группой английских ученых опубликованы данные исследований, в которых отмечено отсутствие четкой связи между размером аденомы гипофиза и головной болью. Важную роль в развитии головной боли играет гормональная активность аденом гипофиза, а также семейная предрасположенность [34].
Массивный супраселлярный рост опухоли может вызвать окклюзионную гидроцефалию (крайне редко) [3,23].
Распространение опухоли латерально в структуры кавернозного синуса может вызывать глазодвигательные нарушения.
Выраженный латеральный рост аденомы в паренхиму медиальных отделов височной доли может провоцировать судорожный синдром.
Супраселлярный рост аденомы гипофиза может вызывать компрессию стебля гипофиза, тем самым, нарушая гипоталамическую ингибицию секреции пролактина. Этот «эффект стебля гипофиза» повышает уровень пролактина в сыворотке крови, маскируясь под пролактиному. Данный клинический синдром более характерен для стебельной краниофарингиомы. Вторично повышенный уровень пролактина, вызванный «эффектом стебля гипофиза», обычно невысокий, и не превышает 150 ng/ml.
Функциональные, или гормонопродуцирующие аденомы гипофиза.
Аденомы гипофиза с клиническими проявлениями гиперсекреции гормонов составляют около 65% всех аденом гипофиза [1,2,8,23].
Клиническая картина гормональноактивных опухолей гипофиза.
Пролактинома. Наиболее часто встречающаяся опухоль. У взрослых женщин в пременопаузе заболевание проявляется овуляторной дисфункцией с ановуляторными циклами, бесплодием; в 90% случаев имеются нарушения менстуального цикла в виде олиго- или аменореи. Дефицит эстрогенов вызывает сухость влагалища, отеки, остеопению. Акне и гирсутизм могут проявляться как дисбаланс между выработкой эстрогенов и андрогенов. Около 80% женщин отмечают снижение либидо, бесплодие, частую смену настроения, галакторею. Женщины в постменопаузальном периоде отмечают снижение либидо и галакторею.
У мужчин заболевание появляется клиникой центрального гипогонадизма, включающего в себя снижение либидо и потенции, бесплодие ввиду олигоспермии, остеопению. Гинекомастия и галакторея у мужчин встречается редко.
Соматотропинома. Специфические появления связаны с развитием акромегалии. Системные проявления включают бивентрикулярную гипертрофию миокарда, диастолическую дисфункцию, аритмии, артериальную гипертензию, эндотелиальную дисфункцию с развитием приобретенной сердечной недостаточности. Респираторные расстройства характеризуются макроглоссией, обструкцией верхних дыхательных путей, вентиляторной дисфункцией, появлением синдрома «ночного апноэ». Метаболические нарушения включают нарушение толерантности к глюкозе, сахарный диабет, гипертриглицеридемию. Имеют место в различной степени выраженности изменения со стороны костей и суставов, захватывающие как позвоночник, так и кости конечностей.
Тиреотропинома. Специфические проявления связаны с развитием синдромом тиреотоксикоза. Для него характерна тахикардия, повышение температуры тела, тремор, экзофтальм, диарея.
Кортикотропинома. Специфические проявления связаны с гиперсекрецией аденокортикотрпного гормона, с развитием болезни Иценко-Кушинга. Характерными проявлениями являются ожирение (по кушингоидному типу), при котором отмечается лунообразное лицо, ожирение туловища, при менее выраженном ожирении конечностей. На туловище имеются стрии (характерно красно-бордового цвета) из-за перерастяжения кожи и ее дистрофии. Отмечается мышечная дистрофия вплоть до развития миопатии. Развивается остеопороз, патологические переломы. Снижен иммунитет. Для детей характерна задержка в росте. При развитии заболевания до или во время пубертатного периода отмечается гипогонадизм и бесплодие: у мужчин снижение либидо и эректильная дисфункция, олигоспермия ввиду низкого уровня содержания тестостерона в крови. У женщин наблюдается олиго- или аменорея, гирсутизм и акне.
Диагностика опухолей хиазмально-селлярной области. Для постановки диагноза необходимо иметь анамнестические сведения о развитии заболевания (особенно важно в педиатрической практике). Кроме этого необходим осмотр невролога, эндокринолога и нейроофтальмолога.
Неврологическое обследование. Необходимо определить уровень сознания, функции черепно-мозговых нервов, сухожильно-периостальные и кожные рефлексы, чувствительную и двигательную сферы, координацию, наличие патологических рефлексов, менингиальную симптоматику. Для диагностики глиом зрительных нервов необходимо исследование зрительных вызванных потенциалов.
Эндокринологическое обследование. Исследуется содержание гормонов гипофиза и периферических эндокринных желез в сыворотке крови: пролактина (ПРЛ), соматотропина (СТГ), аденокортикотропина (АКТГ), лютеинизирующего гормона (ЛГ), фолликулстимулирующего гормона (ФСГ), тиреотропина (ТТГ), инсулиноподобного фактора роста-1 (ИФР-1), кортизола, тироксина, тестостерона, эстрадиола [1,2,8].
Определение кортизола и функции щитовидной железы важно для назначения коррегирующей (заместительной) терапии в до- и послеоперационном периоде. Определение уровня ИФР-1 необходимо, так как он секретируется в печени под влиянием СТГ, и обуславливает тканевое воздействие СТГ. Однократное определение уровня СТГ часто не обладает диагностической ценностью ввиду эпизодической секреции гормона, короткого периода полужизни и перекрестных концентраций СТГ у больных акромегалией и здоровых людей [2,29,40].
Определение уровня гормонов гипофиза является важнейшим тестом в установлении диагноза аденомы гипофиза, установлении гормональной активности опухоли, а также для контроля адекватности медикаментозного лечения, и определения радикальности хирургического лечения аденом гипофиза. Уровень содержания гипофизарных гормонов до начала лечения аденом гипофиза также является прогностическим фактором [2,37].
Нейроофтальмологическое обследование. Выполняется исследование остроты зрения. При выраженной компрессии хиазмы зрительных нервов имеет место характерное нарушение полей зрения в виде выпадения темпоральных отделов полей зрения. Застойные диски зрительных нервов при исследовании глазного дна указывают на внутричерепную гипертензию. Появление или усугубление зрительных нарушений, несмотря на проводимое медикаментозное лечение, указывает на необходимость проведения более агрессивных методов лечения в виде оперативного вмешательства.
Необходим контроль зрительных функций при проведении лечения. Обязательно исследование в до- и послеоперационном периоде в случае выполнения оперативного вмешательства.
Нейровизуализация. Целями нейровизуализации являются определение характера, локализации и распространенности патологического процесса. Определяется размер опухоли, консистенция, наличие кистозного компонента, включений и кровоизлияний в опухоль. Исследуются особенности расположения и локализации, преимущественное направление роста, распространение в структуры основания черепа и их возможную деструкцию. Выявляются взаимоотношения опухоли с артериальными сосудами, желудочками мозга, арахноидальными цистернами, медиобазальными отделами лобной и височной долей. Выявляется наличие и степень выраженности деформации ствола головного мозга [3,13,23,35,10].
Методом выбора при диагностике образований хиазмально-селлярной области является МРТ с контрастным усилением. Преимущества метода: позволяют визуализировать образования размером до 1 мм., что принципиально важно для диагностики функционально активных микроаденом. Возможность четко визуализировать опухолевую ткань и смежные структуры в трех плоскостях. Метод оптимален при исследовании кистозных опухолей, менингиом, аневризм сосудов Велизиева круга, глиом хиазмы. Последние характеризуются однородной плотностью при КТ и изоинтенсивным сигналом на МРТ.
КТ головного мозга. В настоящее время роль КТ в диагностике патологических образований хиазмально-селлярной области ограничена. По диагностической ценности этот метод уступает МРТ, однако является информативным с целью проведения дифференциальной диагностики с образованиями, содержащими кальцинаты или гиперостозы, либо приводящие к деструкции структур основания черепа. Может с успехом применяться при назальной ликворе для визуализации фистулы (метод контрастной цистернофискулографии). Из недостатков следует отметить наличие артефактов Хаунсфилда при исследовании структур основания черепа.
Краниография. Простой и доступный метод. Позволяет визуализировать патологический процесс в области турецкого седла: двухконтурность дна турецкого седла, деструкция передних наклоненных отростков, истончение, деструкция спинки турецкого седла, расширение входа и разрушение дна турецкого седла. Возможно визуализировать гиперостоз при менингиоме, либо кальцинаты при краниофарингиомах.
Одним из методов топической диагностики гормонально активных микроаденом гипофиза является билатеральная катетеризация нижних каменистых или кавернозных синусов с оценкой градиента уровня гормонов. Он основан на том, что венозная система гипофиза обеспечивает независимый сброс крови из каждой половины железы в соответствующий кавернозный синус. При их катетеризации осуществляется забор крови с определением уровня содержания гормона с уже доказанной повышенной секреторной активностью. Наличие градиента концентрации подтверждает локализацию микроаденомы в определенной половине железы. Следует отметить, что эта инвазивная и небезопасная методика не является высокодостоверной. В 40% случаев в норме имеется латерализация оттока крови от гипофиза в правый кавернозный синус, из-за чего диагностические ошибки в определении стороны локализации микроаденом могут достигать 40-60% (при катетеризации соответственно кавернозных и нижних каменистых синусов соответственно) [2,3,37].
Классификация. В нашем обзоре рассматриваются новообразования хиазмально-селлярной области, которые представленные разнородной группой опухолей, объединенных анатомо – топографической локализацией. Каждое из этих образований классифицируется по гистологическому признаку согласно классификации ВОЗ [22,28,36], и представлять полностью эту классификацию в данном обзоре очень громоздко.
Подробно рассмотрим классификацию аденом гипофиза. Они по гистологическому критерию разделяются на: пролактиномы (ПРЛ – секретирующие), соматотропиномы (СТГ – продуцирующие), тиреотропиномы (ТТГ – продуцирующие), аденокортикотропиномы (АКТГ – продуцирующие), гонадотропин - продуцирующие, нуль-клеточные и их варианты, и плюригормональные.
По гормональной активности аденомы гипофиза подразделяются на гормональноактивные и гормональнонеактивные (или нефункционирующие) опухоли.
По размеру выделяют микроаденомы (размер опухоли менее 10 мм во всех измерениях) и макроаденомы (размер опухоли более 10 мм по любому из измерений).
По топографическому расположению и распространению аденомы разделяют на:
- С эндоселлярным ростом.
- С экстраселлярным ростом (около 50% всех опухолей).
- Супраселлярным
- Параселлярным
- Ретроселлярным
- Антеселлярным
- Инфраселлярным
В классификации краниофарингиом выделяют эндосупраселлярные, стебельные (супраселлярные), вентрикулярные (инфундибулярные) и гигантские краниофарингиомы. Гистологически краниофарингиомы подразделяют на адамантинозные и папилломатозные.
Лечение опухолей хиазмально-селлярной области включает в себя медикаментозное, хирургическое и радиологическое [2,3,4,6,8,7,9,10,23,37].
Хирургический метод лечения. В настоящее время транссфеноидальные хирургические вмешательства являются методом выбора при лечении аденом гипофиза и ряда других образований хиазмально-селлярной области [4,13,20]. Различают трансффеноидальный микрохирургический метод, при котором опухоль удаляется при помощи микроскопа, и эндоскопический, при котором используется эндоскопическая техника. Транскраниальные операции применяются при невозможности проведения транссфеноидального вмешательства.
Эндоскопическая техника имеет целый ряд преимуществ перед микрохирургической, так как позволяет проводить операции менее травматично, имеется панорамный обзор операционного поля, всех анатомических ориентиров и образований на всех этапах проведения операции. Наличие сменной угловой оптики эндоскопа дает практически уникальную возможность визуализировать образования, расположенные вне продольной оптической оси тубулярного поля зрения микроскопа. Появляется возможность визуализировать супраселлярную часть опухоли, структуры кавернозного синуса и другие образования. При эндоскопической методике неоценима помощь ассистента, особенно в условиях кровотечения. При выполнении операции с помощью микроскопа возможность для манипуляции на опухоли в глубине раны есть только у оперирующего хирурга [4,6,15,16,18,19].
Стандартный транссфеноидальный эндоскопический подход к турецкому седлу может быть осуществлен эндоназально или сублабиально. Сублабиальный доступ используется в педиатрической практике и при анатомически узких носовых ходах. Во всех остальных случаях используется эндоназальный коридор.
Противопоказания для транссфеноидального доступа [3,4,13]:
1. Выраженный параселлярный рост опухоли с инвазией ее в кавернозный синус (ряд зарубежных авторов отмечает возможность эндоскопического удаления опухоли из кавернозного синуса наличии соответствующего опыта [4,17,39]);
2. Наличие узкой перемычки между супраселлярным и интраселлярным компонентами опухолевого узла (форма «гантели»).
3. Выраженный супраселлярный рост опухоли с прорастанием ее в III желудочек, и паренхиму мозга.
4. Воспалительный процесс в придаточных пазухах носа.
5. Анатомические особенности хирургического коридора: малое турецкое седло, патологическое медиальное смещение сонной артерии.
В остальных случаях применяются транскраниальные доступы, включая субфронтальный, птериональный, их модификации, и некоторые трансбазальные доступы [3,6,10].
В ряде случаев возможно использование двухэтапных операций с применением комбинированных доступов (используются как транссфеноидальный, так и транскраниальный доступы). Выбор тактики в таких случаях обусловлен как анатомо-топографическими особенностями опухоли так и состоянием пациента, и определяется в каждом случае индивидуально, с учетом опыта хирурга.
Лечебные мероприятия при различных опухолях различны, поэтому будут рассмотрены отдельно.
Гормональнонеактивные (нефункционирующие) аденомы гипофиза с наличием масс-эффекта (интра- или экстраселлярного) подлежат хирургическому лечению (метод выбора).
При гормональнонеактивных микроаденомах, не имеющих симптоматики, связанной с объемным воздействием, показано динамическое наблюдение. В случае роста опухоли и появлении масс-эффекта показано хирургическое лечение – транссфеноидальное эндоскопическое удаление опухоли [4,37,29].
Медикаментозная терапия в лечении гормональнонеактивных аденом гипофиза является вспомогательным методом лечения, и направлена на коррекцию нарушенных питуитарных функций.
Гормональноактивные опухоли.
Пролактиномы. Метод выбора в лечении пролактином является медикаментозный с использованием агонистов дофамина. Лечение направлено на нормализацию уровня пролактина, и связанных с ним клинических проявлений, и уменьшение размеров опухоли [1,2,3,31,42].
Следует отметить, что при выявлении микропролактином без выраженных клинических проявлений гиперпролактинемии, они подлежат динамическому наблюдению и контролю (МРТ контроль, уровень пролактина в крови), так как переход микропролактином в макропролактиномы является крайне редким [2].
При неэффективности консервативной терапии, усугублении клинических проявлений (снижение остроты зрения, сужение полей зрения, появление глазодвигательных расстройств, появление или усугубление явлений пангипоитуитаризма, появление или усиление болевого синдрома), увеличении опухоли в размерах, либо кровоизлиянии в опухоль показано хирургическое лечение – удаление опухоли. Хирургическое лечение показано также больным с непереносимостью препаратов медикаментозной терапии [1,2,3,31].
Соматотропиномы. Методом выбора в лечении соматотропином является хирургическое удаление опухоли, независимо от ее размеров [4,33,40,32]. Хирургический метод особенно эффективен при микроаденомах. Если после операции не происходит нормализация биохимических показателей, в качестве дополнительного метода назначается медикаментозная терапия. Препараты – аналоги соматостатина могут назначаться в качестве предоперационной подготовки, либо при наличии противопоказаний к хирургическому лечению. Имеются публикации, посвященные лечению соматотропином препаратом Пегвизомант, представляющим собой продукт генно-инженерного синтеза, и являющийся антагонистом СТГ- рецепторов, и блокатором активности гормона роста [40,42].
Тиреотропинома. Методом первичной терапии является хирургическое лечение. Медикаментозная терапия направлена на поддержание нормального уровня гормонов в послеоперационном периоде [4,23,37].
Аденокортикотропинома. Методом выбора в лечении болезни Иценко-Кушинга или синдрома Нельсона является хирургическое - удаление АКТГ- секретирующей аденомы. При транссфеноидальном (эндоскопическом или при помощи микроскопа) удалении опухоли ремиссия достигается в 70-90% случаев. При макроаденомах, инвазирующих кавернозный синус, хирургическое лечение эффективно в 50-60%. Выполнение билатеральной адреналэктомии в качестве лечебного метода должно производиться при неэффективности хирургического удаления аденомы, и при неэффективности как медикаментозной, так и лучевой терапии [2,4,7,21,23,27,37]. Следует отметить, что лучевое лечение при тяжелых формах болезни Иценко-Кушинга малоэффективно [25,37]. Необходимо отметить, что в ряде случаев при болезни Иценко-Кушинга на МРТ не удается обнаружить микроаденому. Поэтому при исключении эктопированной секреции АКТГ может быть предпринято первичное лучевое лечение [26].
Показаниями для проведения оперативного вмешательства при опухолях хиазмально-селлярной области являются:
Абсолютные показания определяются вне зависимости от гормональной активности опухоли [3,4,13,11,23,37]:
- снижение остроты зрения и сужение его полей, обусловленные сдавлением опухолью зрительного перекреста и зрительных нервов;
- нарушение функции глазодвигательных нервов в связи со сдавлением их опухолью;
- нарушения ликворооттока, гидроцефалия и внутричерепная гипертензия, обусловленные внедрением опухоли в III желудочек;
- кровоизлияние в опухоль;
- ликворея, обусловленная одновременным разрушением опухолью диафрагмы и дна турецкого седла;
- отсутствие эффекта от проводимого консервативного лечения и лучевой терапии.
Хирургическое лечение секретирующих макро- и микроаденом гипофиза показано в следующих случаях [3,4,13,11]:
- кортикотропиномы – болезнь Иценко-Кушинга, синдром Нельсона;
- соматотропиномы – акромегалия;
- пролактиномы – наличие клинических проявлений гиперпролактинемии на фоне отсутствия эффекта от терапии агонистами дофамина, либо при непереносимости медикаментозной терапии;
- тиреотропиномы – прогрессирующий тиреотоксикоз при отсутствии эффекта от консервативного лечения;
- гонадотропиномы – выраженная импотенция или бесплодие (при желательной беременности).
В настоящее время происходит смещение акцента в хирургическом лечении краниофарингиом и менингиом хиазмально-селлярной локализации с открытых методов (использующих субфронтальные, птериональные и их модификации, трансбазальные доступы) на менее травматичные методы которые позволяют более радикально удалять эти опухоли с лучшими послеоперационными результатами. Транссфеноидальному удалению доступны большинство менингиом указанной локализации (исключая обрастание крупных сосудов и вовлечение нервных структур в опухоль), а также инфрадиафрагмальные краниофарингиомы (включая супраселлярное распространение) [17,41,5].
Показания к хирургическому лечению глиом зрительных нервов возникают крайне редко [6,37]. В некоторых случаях эти новообразования могут удаляться в пределах неизмененных зрительных путей, при этом показания к хирургическому лечению, а также и биопсии должны выставляться крайне осторожно.
Общие противопоказания к хирургическому лечению:
- Тяжелое общее состояние больного с декомпенсацией соматических функций.
- Некомпенсированный гипопитуитаризм.
Медикаментозная терапия опухолей хиазмально-селлярной области. Используется в лечении аденом гипофиза, и направлена на подавление функциональной активности гормоносекретирующих аденом, а также на замещение недостаточной выработки питуитарных гормонов [39].
Акромегалия. Цель терапии – подавление секреции гормона роста, и снижение уровня повышенного ИФР-1 в сыворотке крови. Роль медикаментозной терапии необходимо рассматривать как дополнительной в комплексной терапии больныхс акромегалией. Из медикаментозных средств используются:
1) Аналоги соматостатина. Относительно безопасны и эффективны. Угнетают секрецию гормона роста и ИФР-1. Следует отметить, что применение этой группы препаратов необходимо в случаях отказа от хирургического удаления опухоли, когда применяется метод лучевой терапии [2,3,33,40]. В ряде случаев при выраженных клинических проявлениях акромегалии назначается медикаментозное лечение перед плановым хирургическим вмешательством. Показаниями для данной терапии являются поражения желудочно-кишечного тракта, акромегалическая кардиомиопатия, наличие клинически значимого синдрома ночного апноэ, поражения дыхательного тракта, или прогнозируемая трудность при интубации трахеи [32].
2) агонисты дофамина. Их эффективность в лечении акромегалии в настоящее время дискутируется. Применяются в тех же случаях, что описаны выше. Более эффективны в случаях смешанных аденом с повышенным уровнем пролактина в сыворотке крови.
3) Пегвизомант, антагонист рецепторов гормона роста, блокирует периферическую выработку ИФР-1. Является высокоэффективным, однако недостаточно изученным препаратом [33,40].
Пролактиномы. Метод выбора в лечении пролактином в настоящее время является медикаментозный. Из препаратов наиболее эффективными являются агонисты дофамина. Медикаментозное лечение позволяет нормализовать уровень пролактина в сыворотке крови, и контролировать рост опухоли. В случаях резистентности к лечению, или непереносимости препаратов показано хирургическое лечение – удаление опухоли.
Тиреотропиномы. Основной метод лечения хирургический, при его неэффективности, или наличии противопоказаний используется лучевая терапия.
Болезнь Иценко – Кушинга. Медикаментозный метод лечения показан больным только как дополнительный, в сочетании с хирургическим или лучевым лечением. Следует отметить, что в настоящий момент не существует препаратов, подавляющих секрецию АКТГ [26,27]. Лечение носит преимущественно симптоматический характер, хотя используются препараты патогенетической терапии (блокаторы синтеза стероидов в надпочечниках).
Лучевая терапия. Является основным методом лечения глиом зрительных нервов. В лечении аденом гипофиза и менингиом имеет вспомогательное значение, и применяется при неэффективности хирургического и медикаментозного лечения, при наличии противопоказаний к хирургическому лечению, либо при отказе больного от других методов лечения [25,37,33].
Первичная лучевая терапия в настоящее время уступает хирургическому и медикаментозному методу лечения по ряду причин:
- в случае, если необходимо добиться немедленной клинико–биохимической ремиссии (АКТГ- и СТГ- секретирующие опухоли) необходимо применять хирургический метод лечения. В случае лучевого лечения на достижение ремиссии могут потребоваться годы.
- крайне высокая частота (от 30 до 65%) развития гипопитуитарных осложнений после лучевого лечения [8,23,37,25].
ЛИТЕРАТУРА
- Астафьева Л.И., Кадашев Б.А., Калинин П.Л. и др. Клиническая картина, диагностика и результаты первичной медикаментозной терапии больших и гигантских пролактинсекретирующих аденом гипофиза. // Вопросы нейрохирургии. – 2008 № 4 С. 36-39.
- Вакс В.В., Дедов И.И. Возможности медикаментозной терапии опухолей гипофиза. // Вопросы нейрохирургии. – 2005 № 2 С. 30-37.
- Кадашев Б.А. Аденомы гипофиза: клиника, диагностика, лечение. – Тверь, 2007.
- Калинин П.Л. Эндоскопическая транссфеноидальная хирургия аденом гипофиза и других опухолей околоселлярной локализации: автореф. дисс. …д-ра мед. наук. – М., 2009.
- Калинин П.Л., Фомичев Д.В., Кутин М.А., Кадашев Б.А., Файзуллаев Р.Б. Расширенные эндоскопические эндоназальные транссфеноидальные доступы в хирургии основания черепа. // Журнал «Вопросы нейрохирургии имени Н.Н. Бурденко». – 2008. - №4, стр. 47 – 49.
- Коновалов А.Н., Черекаев В.А., и др. Хирургия основания черепа. ПБОЮЛ Андреева Т.М. М., 2004.
- Марова Е.И, Арапова С.Д., Трунин Ю.К., Колесникова Г.С, «Ранние и отдаленные результаты нейрохирургического лечения БИК», Проблемы эндокринологии, 2006, Т.52, №4, 1,3, 6-10.
- Нейроэндокринология. Клинические очерки, под редакцией Маровой Е.И.– Ярославль, 1999, стр.81-144.
- Практическая нейрохирургия. Руководство для врачей. Под ред. Б.В. Гайдара. – С Пб., 2002.
- Тиглиев Г.С., Олюшин В.Е., Кондратьев А.Н. Внутричерепные менингиомы. Санкт-Петербург, 2001.
- Фомичев Д. В. Эндоскопическое эндоназальное удаление аденом гипофиза (анатомическое обоснование, методика проведения операций и послеоперационные результаты): Автореф. дис. ... канд. мед. наук. — М., 2007.
- Черебилло В. Ю., Гофман В. Р., Полежаев А. В. Трансфеноидальная хирургия больших и гигантских аденом гипофиза с применением интраоперационного эндовидеомониторинга // Вопр. нейрохир. — 2005. — № 1. — С. 12—15.
- Черебилло В.Ю. Транссфеноидальная эндоскопическая хирургия в комплексном лечении аденом гипофиза: автореф. дисс. …д-ра мед. наук. – С-Пб., 2007.
- Biousse V, Newman N.J., Oyesiku N.M. Precipitating factors in pituitary apoplexy. J Neurol Neurosurg Psychiatry 2001; 71:542–545.
- Cappabianca P., Cavallo L.M., de Divitiis E., Endoscopic Endonasal Transsphenoidal Surgery. Neurosurgery 55: 933 - 941, (2004).
- Cappabianca P., de Divitiis E.: Endosccopy and transsphenoidal surgery. Neurosurgery 54:1043-1050, 2004.
- Cavallo LM., Prevedello D., Esposito F., Laws ERJr., Dusick JR., Messina A., Jane JAJr. Kelly DF., Cappabianca P. The role of the endoscope in the transsphenoidal management of cystic lesions of the sellar region. Neurosurg Rev (2008) 31:55-64.
- de Divitiis, E; Сappabianca P eds.: Endoscopic Endonasal Transsphenoidal Surgery. Springer-Verlag Wien New York, pp.198, (2003).
- de Divitiis, E; Сappabianca P: Endoscopic endonasal transsphenoidal surgery. In: Advances and Technical Standards in Neurosurgery (Pickard, JD; ed). Springer-Verlag Wien New York, 27: 137-177, (2002).
- de Divitiis, E; Сappabianca P; Cavallo, LM: Endoscopic Transsphenoidal Approach: Adaptability of the procedure to different sellar lesions. Neurosurgery 51: 699-707, (2002).
- Dehdashti A.R., Gentili F. Current state of the art in the diagnosis and surgical treatment of Cushing disease: early experience with a purely endoscopic endonasal technique. Neurosurg Focus 23 (3):E9, 2007.
- DeLellis R.A., Lloyd R.V., Heitz P.U., Eng. C. (eds.) (2004) World Health Organization classification of tumors: Numours of endocrine organs. IARC, Lyons.
- Diagnosis and Management of Pituitary Tumors, - K. Thapar, K. Kovacs, B.W. Scheithauer, R.V. Lloyd, Humana press, Totowa, New Jersey, 2001.
- Endoscopic transsphenoidal pituitary surgery / Teramoto A. // Program and materials / Russian – Japanese neurosurgical symposium. - St-Peterburg, 2008. - P. 71.
- Ghostine S., Ghostine M.S., Johnson W.D. Radiation therapy in the treatment of pituitary tumors. Neurosurg Focus 24 (5):E8, 2008.
- Jagannathan J., Sheedan J.P., Jane J.A.Jr.; Evaluation and management of Cushing syndrome in cases of negative sellar magnetic resonance imaging. Neurosurg Focus 23 (3):E3, 2007.
- Kelly D. F. Transsphenoidal surgery for Cushing’s disease: a review of success rates, remission predictors, management of failed surgery, and Nelson’s Syndrome. Neurosurg Focus 23 (3):E5, 2007.
- Kleihues P., Cavenee W.K. (ed.) Tumors of the Nervous System. Pathology and Genetics: World Health Organization International Classification of Tumors. Lyon, France: WHO/IARC, 2000.
- Kurosaki M., Ludecke D.K., Flitsch J., Saeger W. Surgical Treatment of Clinically Nonsecreting Pituitary Adenomas in Elderly Patients. Neurosurgery 47:843–849, 2000.
- Lad S.P., Patil C.G., Laws E.R.Jr., et all; The role of inferior petrosal sinus sampling in the diagnostic localization of Cushing’s disease. Neurosurg Focus 23 (3):E2, 2007.
- Liu J.K., Couldwell W.T. Contemporary management of prolactinomas. Neurosurg Focus 16 (4):Article 2, 2004.
- Melmed S., Casanueva F.F., Cavagnini F. et al. Consensus statement: medical management of acromegaly. European Journal of Endocrinology (2005) 153 737–740.
- Melmed S., Casanueva F.F., Cavagnini F. et al. Guidelines for Acromegaly Management. J Clin Endocrinol Metab, September 2002, 87(9):4054–4058.
- Miles J. Levy M.J., Jager H.R., Powell M., Matharu M.S. Pituitary Volume and Headache. Size Is Not Everything. Arch Neurol. 2004;61:721-725.
- Moore A.F., Grinspoon S.K. Image in endocrinology: A Dural Tale. The Journal of Clinical Endocrinology & Metabolism 92(9):3367–3368.
- Naoko Sanno, Akira Teramoto, R. Yoshiyuki Osamura et all., Pathology of pituitary tumors. Neurosurg Clin N Am 14 (2003) 25–39.
- Neuro-oncology of CNS Tumors, J.-C. Tonn, M. Westphal, J.T. Rutka, S.A. Grossman, Springer, Berlin, 2006.
- Pirris SM, Pollack IF, Snyderman CH, Carrau RL, Spiro RM, Tyler-Kabara E, Kassam AB. Corridor surgery: The current paradigm for skull base surgery. Childs Nerv Syst 23(4), 377-384, 2007.
- Prabhakar V.K.B., Shalet S.M.. Aetiology, diagnosis, and management of hypopituitarism in adult life. Postgrad. Med. J. 2006; 82; 259-266.
- Trainer P.J., Drake W.M., Katznelson L, et. al. Treatment of acromegaly with the growth hormone-receptor antagonist Pegvisomant. N Engl J Med 2000; 342:1171-1177.
- Transnasal - transsphenoidal tumor extirpation for the infradiaphragmatic craniopharyngiomas / Abe T., Leudecke D.K. // Program and materials / Russian – Japanese neurosurgical symposium. - St-Peterburg, 2008. - P. 72 - 74.
- Vance M.L. Treatment of patients with a pituitary adenoma: one clinican's experience. Neurosurg Focus 16 (4):Article 1, 2004.
- Verrees M., Arafah B.M., Selman W.R. Pituitary tumor apoplexy: characteristics, treatment, and outcomes. Neurosurg Focus 16 (4):Article 6, 2004.
| Нейрохирург в Минске Журавлев Владимир Анатольевич | Нейрохирург в Минске Шанько Юрий Георгиевич |
Может ли микроаденома гипофиза влиять на зрение и невозможность зачать ребёнка?
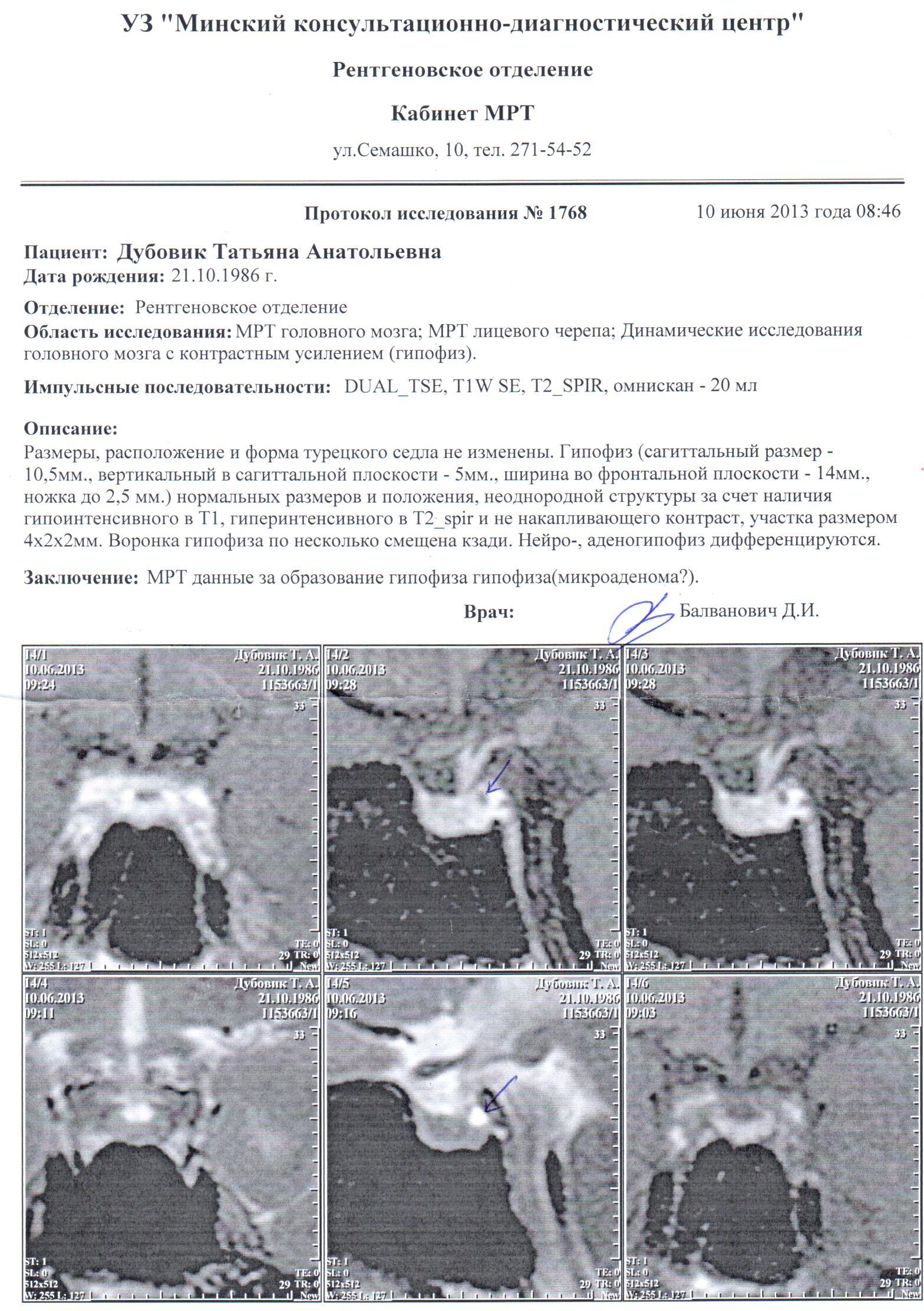
Я из Минска, 26 лет, бесплодие, миопия высокой степени. С 7 лети начало портиться зрение, с 12 лет месячные нерегулярные, задержки были до 7 месяцев. Лечилась от бесплодия, диагноз СПКЯ. Недавно сделала МРТ гипофиза, микроаденома гипофиза. пролактин в норме. Может ли микроаденома влиять на зрение и невозможность зачать ребёнка?
Обследование по поводу бесплодия не начинается с МРТ (КТ) исследования. Около 30% причин бесплодия заключается в эндокринных проблемах. Необходимо определить, в первую очередь, есть ли у Вас овуляция. Проверить уровень тиротропного гормона и некоторых других. Начните с консультации эндокринолога или эндокринолога-гинеколога. И только после того, как у врача появятся мысли о причинах Вашего бесплодия, можно будет говорить о КТ или МРТ. P.S. Около 20% здоровых молодых девушек по данным МРТ имеют микроаденомы гипофиза.