Тактика лечения при острой перфорации правого желудочка электродом электрокардиостимулятора

Развитие интервенционной кардиологии за последние два десятилетия обусловлено поиском новых методов оказания помощи при острых расстройствах сердечного ритма и коронарного кровотока. Однако увеличение числа инвазивных процедур, к которым также относится имплантация электрокардиостимулятора, безусловно, приводит к росту ятрогенных осложнений, некоторые из них являются угрожающими жизни [1, 25].
В настоящее время частота острых перфораций составляет, по разным источникам, 0,1—0,8% для кардиостимуляторов и 0,6—5,2% для имплантируемых кардиовертеров-дефибрилляторов [12, 22].Разработка и внедрение в клиническую практику современных электродов, отличающихся меньшим диаметром и большей гибкостью, обусловили снижение риска перфорации миокарда [4, 17, 18]. Согласно данным регистра компании Boston Scientific, 2/3 перфораций происходят в течение первой недели после имплантации электрода, а 1/3— позднее. Тип фиксации электрода на это соотношение не влияет. При этом отмечено, что поздние перфорации возникают довольно редко и трудны для выявления [11, 18].
Перфорация миокарда правого предсердия встречается в 2—3 раза чаще, чем перфорация правого желудочка, что объясняется различной толщиной стенок указанных камер сердца. Высокая частота перфораций миокарда у пациентов с имплантируемыми кардиовертерами-дефибрилляторами, по сравнению с кардиостимулятором, вероятнее всего связана с «жесткостью» электрода [4, 8, 18]. Основным фактором риска перфорации миокарда является тип фиксирующего устройства эндокардиального электрода. В настоящее время существует 3 основных типа фиксирующего устройства: электрод с активной фиксацией типа «буравчик»; электрод с активной фиксацией типа «якорь»; электрод с пассивной фиксацией. Наиболее часто (0,121%) перфорации миокарда происходят при установке электрода типа «буравчик», для двух других электродов этот показатель составляет 0,019 и 0,012% соответственно [2, 3, 4, 12].
Кроме размеров контактной части электрода, существует ряд других факторов, способствующих перфорации миокарда.
К ним относятся [4, 5, 15, 25]:
— толщина свободной стенки миокарда;
— применение стероидных препаратов в течение 7 дней перед имплантацией электрода;
— возраст пациента;
— женский пол;
— состояние гипокоагуляции;
— индекс массы тела менее 20;
— жесткость электрода/стилета;
— использование временного кардиостимулятора;
— количество репозиций электрода.
Острые перфорации миокарда, как правило, характеризуются яркой клинической картиной, в то время как каждые 15 из 1000 поздних перфораций протекают бессимптомно и выявляются при оценке функции кардиостимулятора [6, 10].
Основными клиническими признаками являются [4, 5, 7, 13, 19, 21, 23]:
— боль в грудной клетке;
— ощущение стимуляции мышц;
— гемопневмоторакс;
— перикардит;
— гипотония.
Следует отметить, что большинство перфораций миокарда не приводит к тампонаде сердца за счет закрытия дефекта электродом и мышечных сокращений [2, 12].
Диагностика перфораций миокарда сложна и основывается на оценке как клинических, так и инструментальных данных. Электрокардиография позволяет выявить лишь нарушения функции кардиостимулятора [3, 9]. Проведение эхоКГ направлено в первую очередь на диагностику гемоперикарда и тампонады [17, 20, 22, 23]. Основными методами диагностики данного осложнения являются рентгенологические. Нередко бывает достаточным проведение рентгенографии органов грудной клетки для выявления положения электрода за пределами тени сердца [14, 24]. Самым ценным методом диагностики перфораций является компьютерная томография, которая помогает наиболее точно определить локализацию электрода и дальнейшую тактику [14, 22].
Выявленный с помощью программатора высокий порог стимуляции сердца чаще всего свидетельствует о перфорации миокарда. Однако нормальные показатели сопротивления электрода и параметры стимуляции не исключают возможности перфорации. В случае неглубокой перфорации катод может располагаться проксимально к эпикарду, а анод — проксимально или внутри электрода, приводя к нормальным показателям работы кардиостимулятора [12, 16, 24, 26].
Лечебная тактика
В настоящее время не существует однозначного мнения относительно тактики лечения данной категории пациентов [6, 12, 26]. В случае острой перфорации, как правило, выполняют репозицию электрода с серией последующих эхокардиографичеких исследований, отслеживая наличие выпота в полости перикарда. Необходимость хирургического закрытия дефекта миокарда в данной ситуации возникает редко [23].
При поздней перфорации репозиция электрода может быть довольно рискованной в связи с тем, что он сокращается вместе с тканями сердца [5, 11, 16].
Удаление электродов с активной фиксаций типа «буравчик» производят путем первоначального ввинчивания фиксирующей спирали, если это удается, а затем проводят его экстракцию. Электроды с активной фиксацией типа «якорь», имеющие контактную часть большего диаметра, извлекают поэтапно. Вначале удаляют контактную часть, снижая тем самым риск кровотечения и повреждения мягких тканей при экстракции, а затем, используя чрезвенозный доступ, вытягивают оставшуюся часть электрода [11, 12, 18].
Профилактика
Снижение риска перфорации миокарда достигается с помощью следующих условий:
— использование электродов с пассивной фиксацией;
— имплантация электрода к перегородке сердца, особенно у
пациентов с истонченными стенками сердца;
— осторожность при выполнении замены временного электрода на постоянный.
В случае использования электродов с активной фиксацией типа «буравчик» следует избегать избыточных поворотов электрода, а также частично удалить стилет с целью уменьшения силы, применяемой при установке дистального конца электрода [13—15, 24].
Извлечение электрода должно производиться строго в кардиохирургической операционной под контролем чреспищеводной эхоКГ и по возможности рентгеноскопии [16, 17, 21].
Клинический случай.
Больная 68 лет поступила в кардиохирургическое отделение с направительным диагнозом: синдром слабости синусового узла, тахи-брадиформа. Пароксизмальная форма фибрилляции предсердий.
В плановом порядке по поводу настоящего заболевания пациентке был имплантирован электрокардиостимулятор («Guidant Insignia Entra DR») с биполярными электродами и активной фиксацией («Flextend 2»).
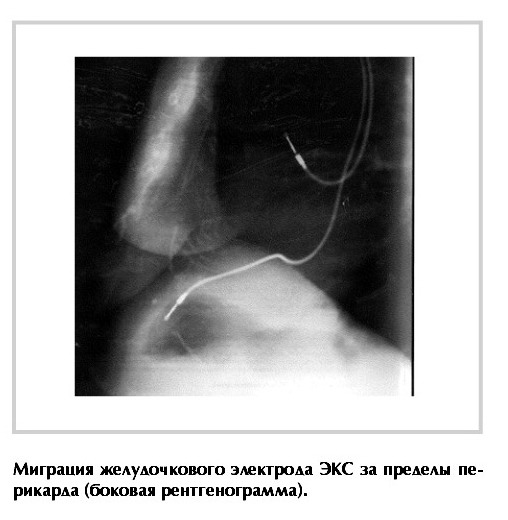
Ранний послеоперационный период протекал гладко. Однако на 3-и сутки после операции появились жалобы на боль в области левого подреберья и ощущение сокращений диафрагмы. При оценке работы ЭКС с помощью программатора выявлено нарушение чувствительности желудочкового электрода. Параметры стимуляции правого желудочка: амплитуда 2,5 В, длительность импульса 0,25 мс. Выполнено перепрограммирование кардиостимулятора в режим ААI, на фоне чего пациентка перестала ощущать мышечные сокращения диафрагмы. При рентгенографии органов грудной клетки четко определялась миграция желудочкового электрода за пределы перикарда (см. рисунок). Трансторакальная и ЧП эхоКГ: выпота в полости перикарда не обнаружено. Четко визуализируется миграция желудочкового электрода за пределы перикарда.С целью более точного определения локализации желудочкового электрода пациентке выполнена компьютерная томография органов грудной клетки, на которой выявлено расположение электрода в толще диафрагмы.
На фоне работы кардиостимулятора в режиме AAI электрод, перфорировавший стенку правого желудочка, было решено не удалять. Проводилось динамическое наблюдение. Учитывая отсутствие стимуляции правого желудочка, пациентке имплантировали новый желудочковый электрод («Flextend 2») в область миокарда межжелудочковой перегородки. На контрольной рентгенограмме и при эхокардиографических исследованиях определялось нормальное положение вновь установленного желудочкового электрода. Выпота в полости перикарда не отмечалось. При оценке работы кардиостимулятора с помощью программатора определяется ее адекватность.
Пациентка была выписана на 10-е сутки после операции. В последующем во время планового осмотра через 2 мес после имплантации стимулятора у больной определяется адекватная работа кардиостимулятора в режиме DDDR. Положение электродов на рентгенограмме органов грудной клетки без существенной динамики по сравнению с предыдущим.
Приведенное клиническое наблюдение демонстрирует актуальность активно-выжидательной тактики в случае перфорации электродом камер сердца. При нахождении электрода внутри средостения и отсутствии данных, свидетельствующих о кровотечении, целесообразна имплантация дополнительного электрода без экстракции предыдущего. При развитии кровотечения или гнойных осложнений, высоком риске угрожающих жизни повреждений магистральных сосудов, легочной ткани необходимо удалить электрод.
ЛИТЕРАТУРА
1. Селиваненко В.Т., Мартаков М.А., Пономарев Е.В. и др.Хирургическое лечение больного с перфорацией правого предсердия и легкого электродом для наружной электрокардиостимуляции вследствие его перелома и миграции. Вестн хир 2005; 3: 63.
2. Aoki O.J., Takigami K., Kubota S., Shingu Y.Surgical treatment of ventricular and pericardial perforation by a permanent pacing lead: A case report. J Cardiol 2005; 45: 69—73.
3. Danik S.B., Mansour M., Singh J. et al. Increased incidence of subacute lead perforation noted with one implantable cardioverter-defibrillator. Heart Rhythm 2007; 4: 439—442.
4. Ellenbogen K.A., Wood M.A. Techniques of pacemaker implantation and removal. In: Cardiac pacing and ICDs, 4th edition, Ellenbogen KA (ed.). Blackwell Publishing Oxford 2005; 5: 218.
5. Ellenbogen K.A., Wood M.A., Shepard R.K. Delayed complications following pacemaker implantation. Pacing Clin Electrophysiol 2002; 25: 1155—1158.
6. Fisher J.D., Fox M., Kim S.G. et al. Asymptomatic anterior perforation of an ICD lead into subcutaneous tissues. Pacing Clin Electrophysiol 2008; 31: 1: 7—9.
7. Greenberg S., Lawton J., Chen J. Right ventricular lead perforation presenting as left chest wall muscle stimulation. Circulation 2005; 111: 451—452.
8. Greendberg S., Lawton J., Chen J. Right ventricular lead perforation presenting as left chest muscle stimulation. Circulation 2005; 111: 451—452.
9. Hirschl D.A., Jain V.R., Spindola-Franco H. et al. Prevalence and characterization of asymptomatic pacemaker and ICD led perforation on CT. PACE 2007; 30: 28—32.
10. Hirschl D.A., Jain V.R., Spindola-Franco H. et al. Prevalence and char-acterization of asymptomatic Pacemaker and ICD lead perforation on CT. Pacing Clin Electrophysiol 2007; 30: 28—32.
11. Khan M.N., Joseph G., Khaykin Y. et al. Delayed lead perforation: A disturbing trend. PACE 2005; 28: 251—253.
12. Krivan L., Kozak M., Vlasinova J., Sepsi M. Right Ventricular Perforation with an ICD Defibrillation Lead Managed by Surgical Revision and Epicardial Leads—Case Reports. Department of Cardiology, University Hospital Brno, Czech Republic 2008; 31: 3—6.
13. Laborderie J., Bordachar P., Reuter S., Clémenty J. Myocardial pacing lead perforation revealed by mammary hematoma next to the device pocket. J Cardiovasc Electrophysiol 2007;
14: 338. Merla R., Reddy N.K., Kunapuli S. et al. Late right ventricular perforation and hemothorax after transvenous defibrillator lead implantation. Am J Med Sci 2007; 334: 3: 209—211.
15. Molina J.E. Perforation of the right ventricle by transvenous defibrillator leads: prevention and treatment. Pacing Clin Electrophysiol 1996; 19: 3: 288—292.
16. Nägele H., Behrens S., Azizi M. What can happen during coronary sinus lead implantation: dislocation, perforation and other catastrophes. Herzschrittmacherther Elektrophysiol 2007; 18: 4: 243—249.
17. Saksena S. Defibrillation tresholds and perioperative mortality associated with endocardial and epicardial defibrillation lead systems. The PCD investigators and participating institutions. Pacing Clin Electrophysiol 1993; 16: 202—207.
18. Sanoussi A., Nakadi B. Lardinios I. et al. Late right ventricular perforation after permanent pacemaker implantation: How far can the lead go? PACE 2005; 28: 723—725.
19. Sestito A., Sgueglia G.A., Infusino F. et al. A 60 year old man with chest pain following pacemaker implantation. J Ayub Med Coll Abbottabad 2005; 172: 874.
20. Singhal S., Cooper J.M., Cheung A.T., Acker A.M. Rib perforation from a right ventricular pacemaker lead. Circulation 2007; 115: 391—392.
21. Sivakumaran S., Irwin M.E., Gulamhusein S.S., Senaraine P.J.M. Pospacemaker implant pericarditis: Incidence and outcomes with active fixation leads. Pacing Clin Electrophysiol 2002; 25: 833—837.
22. Spencker S., Mueller D., Marek A., Zabel M. Severe pacemaker lead perforation detected by an automatic home-monitoring system. Eur Heart J 2007; 28: 1432.
23. Srivathsan K., Byrne R.A., Appleton C.P., Scott L.R.P. Pneumopericardium and pneumothorax contralateral to venous access site after permanent pacemaker implantation. Europace 2003; 5: 361—363.
24. Tran N.T., Zivin A., Mozaffarian D., Karmy-Jones R. Right atrial perforation secondary to implantable cardioverter defibrillator insertion. Can Respir J 2001; 8: 4: 283—285.
25. Vidal M.C., Cuesta P., Vázquez E. et al. Cardiac perforation as a late complication in a man with an implantable cardioverter-defibrillator. Rev Esp Anestesiol Reanim 2008; 55: 2: 115—118.
26. Williams J.M., Rock D.T., Pabst S.J. et al. Clinical experience with the implantable cardioverter defibrillator. Ann Thorac Surg 1994; 58: 4: 1297—1303.
Уровень смертности при обмороках сердечного происхождения достигает 10 %.

50-летнюю Нину Михайловну «скорая» привезла в больницу с диагнозом судороги. Она проснулась среди ночи с сильной болью в животе. На глазах у мужа стала пепельно-серой, буквально обливалась потом… И тут вдруг потеряла сознание. Перестала дышать. Только через пару минут постепенно стала приходить в себя. Муж Нины Михайловны рассказал врачам, что судорог и прикусов языка во время и после приступа у жены не было, как не было и послеобморочной спутанности сознания. Сказал еще, что несколько лет назад, когда у нее свело икроножную мышцу, она точно так же теряла сознание.
После обследования пациенте поставили диагноз: сосудистый обморок, спровоцированный болью.
Второй случай. Пенсионер Даниил Ильич в последние месяцы падал в обморок даже несколько раз. Все начиналось со звона в ушах, и потом он на секунды отключался. Тут надо сказать и о прошлом «опыте» мужчины: два инфаркта, один инсульт.
После последнего обморока больного госпитализировали. У него был очень редкий пульс. Пациента уложили на койку, а вскоре он пробормотал медсестре: «Я ухожу…» На ЭКГ-мониторе в тот момент была долгая пауза — отсутствие сокращений сердца… Сейчас Даниил Ильич живет с водителем ритма — электрокардиостимулятором, который обеспечивает ему пульс нужной частоты.
Людей с обмороками не так и мало. И часто врачи в замешательстве: необъяснимые потери сознания. Могут, например, списать на трудноизлечимую эпилепсию. Тогда, увы, больные лечатся с неверным диагнозом. Очень часто таким диагнозом страдают дети.
У 12-летнего Никиты с пяти лет частые обмороки. Все это время он наблюдался у неврологов как эпилептик. Получал противосудорожные препараты, все большими и большими дозами. Без эффекта. При плановом медосмотре электрокардиограмма ребенка привлекла внимание аритмологов. Оказалось, эпилепсия тут ни при чем. Причина — в электрической аномалии в сердце. А проявляется она так: сердце иногда полностью останавливается, обычно после «залпов» быстрого, до 200 ударов в минуту, пульса. Теперь Никите помогает имплантированный кардиовертер-дефибриллятор. Прибор распознает опасные аритмии и тут же прерывает их, не давая сердцу «захлебнуться» в патологическом ритме.
Итак, обморок. Все знают, что это такое, но не все знают, почему так происходит. Потому что мозг вдруг не получает достаточно крови и кислорода. Почти у 50 % взрослых хотя бы раз в жизни случался обморок (кстати, его медицинский термин — синкоп). Вообще, из всех пациентов, обращающихся за неотложной помощью, больше 3 % — те, кто страдает синкопальными состояниями. Конечно, случаются обмороки и у почти здоровых людей. Провоцируются они, например, сильным испугом, болью, духотой, переутомлением, нагрузками. Но есть и куда более серьезные «провокаторы». В 10 % случаев за обмороками скрываются болезни сердца: кардиомиопатия, миокардит, врожденный порок сердца, а еще так называемые первичные электрические болезни сердца, при которых без явных признаков поражения сердечной мышцы может развиться жизнеугрожающая аритмия, говорит хирург, аритмолог, кардиолог 9-й клинической больницы Минска Сергей Моисеенко (на снимке).
Уровень смертности при обмороках сердечного происхождения достигает 10 % (более половины их связано с аритмией). В случае невыясненных причин синкопальных состояний смертность — 36,6 %.
Пациенты после обморока госпитализируются с самыми разными диагнозами. Определить истинные причины случившегося, утверждают доктора, порой непросто даже после тщательнейшего обследования. И в 25 % случаев эти причины остаются, увы, так и невыясненными, а пациент продолжает при этом сильно рисковать. Рискует, например, развить жизнеугрожающую аритмию, что может закончиться синдромом внезапной смерти. Или получить рецидивы пусть и менее фатальных, но тоже опасных обмороков. Наконец, при потере сознания можно попросту травмироваться. Упал, очнулся — разбитая голова. Или же представьте: человек «нырнул» в обморок прямо на рабочем месте, а работа его связана с высотой или движущимися механизмами...
Как видно, обмороки — проблема серьезная. А раз есть проблема — должно быть и решение, то есть своевременная диагностика и выбор правильной терапии этого опасного явления.
— Создать центр обморочных состояний — эту идею я вынашиваю несколько лет. В России, например, подобное учреждение работает уже давно, — рассказывает Сергей Моисеенко. — Есть идеи организовать такой центр на базе 9-й больницы или Минского консультационно-диагностического центра. Планируется привлечь специалистов, диагностические службы и оборудование из разных клиник. Пока в стране нет отдельных специалистов, занимающихся именно обмороками, а в кадровом реестре нет и такой специальности, как синкополог.
Даже после полного осмотра пациенту центра, если понадобится, назначат дополнительные исследования. То есть врачи будут делать все, чтобы определить-таки истинную причину болезни. А в случаях, когда в короткие сроки это сделать все же не удастся, пациента внесут в специальную базу данных, он будет регулярно наблюдаться специалистами до тех пор, пока не определят природу его синкопальных эпизодов. Ни один не уйдет после обследования, не получив ответов на свои вопросы, подчеркивает Сергей Моисеенко.
Сейчас создается виртуальный прототип центра. Он соберет внушительную библиотеку материалов, посвященных проблеме обмороков. Люди смогут бесплатно проконсультироваться онлайн, расшифровать ЭКГ и получить разную информацию о своем сердечно-сосудистом здоровье.

