Взаимосвязь цереброгенных аритмий сердца с нарушениями функциональной активности головного мозга

У больных с заболеваниями головного мозга часто выявляются нарушения ритма и проводимости сердца, приводящие к значительному ухудшению качества жизни и в существенной мере усугубляющие течение и прогноз основного неврологического заболевания [1-3]. К примеру, сердечная аритмия признается одной из наиболее вероятных причин внезапной смерти при эпилепсии [4, 5]. Установлено, что в возникновении цереброгенных аритмий сердца ведущую роль играет дисфункция надсегментарных вегетативных центров, сопровождающаяся выбросом катехоламинов и/или прямой активацией вегетативных сердечных нервов [6-10]. В ряде работ показана связь нарушений ритма и проводимости сердца с изменениями биоэлектрической активности головного мозга [11-20], но конкретные механизмы взаимоотношений нарушений биоэлектрической активности головного мозга с различными видами цереброгенных аритмий сердца являются очень сложными и недостаточно изученными.
Целью настоящего исследования явилось изучение особенностей нарушений ритма и проводимости сердца у больных с органической патологией головного мозга в контексте имеющихся у них нарушений биоэлектрической активности головного мозга.
Материалы и методы.
Обследовано 49 больных (32 мужчины и 17 женщин) в возрасте от 16 до 49 лет (средний возраст - 27,2 ± 7,3 года) с органической патологией головного мозга, в том числе с эпилепсией - 34 больных, с последствиями закрытой черепно-мозговой травмы (ЗЧМТ) - 10, с последствиями воспалительных заболеваний головного мозга (ВЗГМ) - 3, с опухолями головного мозга - 2 больных. Рассматриваемые больные не имели органической патологии сердечно-сосудистой системы.
Обследование включало запись ЭКГ в 12 отведения (компьютерный электрокардиограф Decard-12), холтеровское мониторирование ЭКГ в течение 24 часов (Икар 2.03), компьютерную электроэнцефалографию (ЭЭГ) (компьютерный электроэнцефалограф DX-NT), синхронную регистрацию ЭЭГ и ЭКГ (компьютерный электроэнцефалограф DX-NT). Регистрация ЭЭГ включала 7 последовательных проб по 1 минуте каждая: 1) фоновая запись; 2) запись с открытыми глазами; 3-5) гипервентиляция 1-3 мин; 6) низкочастотная фотостимуляция с частотой 2 Гц; 7) высокочастотная фотостимуляция с частотой 16 Гц. При определении типа ЭЭГ использовалась классификация Е.А. Жирмунской [21].Синхронная регистрация ЭЭГ и ЭКГ осуществлялась в течении 10 минут и включала запись в состоянии покоя и во время проведения функциональных проб (гипервентиляция в течении 3-х минут, высокочастотная и низкочастотная фотостимуляция).
Для оценки степени взаимосвязи нарушений ритма и проводимости сердца с нарушениями биоэлектрической активности головного мозга проводился анализ таблиц сопряженности по ряду параметров, включая тип ЭЭГ, наличие и локализацию эпилептиформной и условно эпилептиформной активности, локализацию медленной активности, вид аритмии. Мерой величины связи признаков считался коэффициент сопряженности (С), значимость связи оценивалась по критерию хи-квадрат Пирсона с поправкой Йетса (py). Достоверность различий определялась на основании двустороннего точного критерия Фишера (pf). Результаты обрабатывались с помощью пакета прикладных статистических программ STATISTICA for Widows 5.0 (StatSoft, Inc).
Результаты и обсуждение.
При стандартной записи ЭКГ и холтеровском мониторировании ЭКГ нарушения ритма и проводимости сердца выявлены у 40 из 49 больных (81,6%) с заболеваниями головного мозга (таблица 1). Преобладающими нарушениями были суправентрикулярная непароксизмальная тахикардия (СВНТ) (14 больных/28,6%), суправентрикулярная экстрасистолия (СВЭ) (13 больных/26,5%), синоатриальные блокады II степени I типа (САБ) (9 больных/18,4%), выраженная синусовая брадикардия (ВСБ) (8 больных/16,3%) и желудочковая экстрасистолия (ЖЭ) (7 больных/14,3%). У 24 больных (49%) одновременно регистрировались от 2 до 6 различных видов аритмий. У 9 больных (18,4%) нарушения ритма и проводимости сердца не выявлялись.
Нарушения биоэлектрической активности головного мозга имели место практически у всех обследованных больных (таблица 2). Преобладали диффузные изменения ЭЭГ в виде дезорганизации альфа-активности, уменьшения её выраженности, сглаженности или отсутствия зональных различий, увеличения индекса и амплитуды медленной активности (дезорганизованный тип ЭЭГ) (24 больных/49%) или в виде выраженной десинхронизации с уменьшением или полным исчезновением альфа-активности, увеличением числа бета-колебаний и уменьшением общего амплитудного уровня кривой ЭЭГ (десинхронный тип ЭЭГ) (20 больных/40,8%). У 28 больных (57,1%) отмечались генерализованные вспышки высокоамплитудных волн в альфа-, тета- и дельта-диапазонах, расцениваемые как условно эпилептиформные феномены, у 9 больных (18,4%) регистрировалась эпилептиформная активность в виде разрядов острых волн, пиков, комплексов пик-волна и острая-медленная волна. У 8 больных (16,3%) имелись признаки локальной патологии в виде регулярной фокальной тета- или дельта-активности.
Таблица 1. Частота и структура нарушений ритма и проводимости сердца у больных с органической патологией головного мозга.
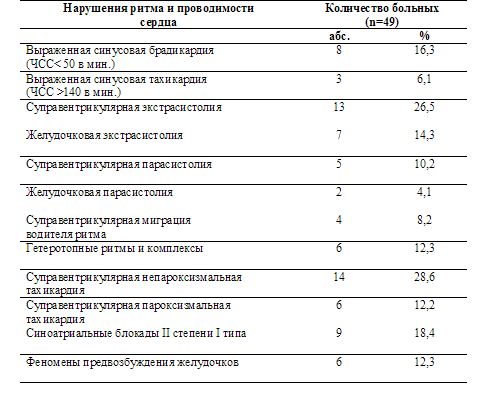
Таблица 2. Характеристика ЭЭГ больных с органической патологией го-ловного мозга.

Фокальная эпилептиформная активность регистрировалась у 5 больных (10,2%), из них 4 больных имели один очаг активности, локализовавшийся в лобной или височной доле слева или справа, а у 1 больного эпилептиформная активность регистрировалась одновременно в лобной и височной долях справа. Обращали на себя внимание бóльшая частота и разнообразие нарушений сердечного ритма у больных с правосторонней локализацией очага (3 больных), включавшие СВЭ, суправентрикулярную и желудочковую парасистолию, параксизмальную и непароксизмальную суправентрикулярную тахикардию, у больных же с левосторонней локализацией очага (2 больных) нарушения ритма ограничивались суправентрикулярной миграцией водителя ритма и СВНТ.
У больных без аритмий сердца преобладающим типом ЭЭГ был десинхронный тип (5 больных), реже встречались дезорганизованный и организованный типы ЭЭГ (у 3 и 1 больного соответственно). У 3 больных выявлялись условно эпилептиформные феномены, у 1 больного - явная эпилептиформная активность. По параметрам биоэлектрической активности головного мозга группа больных без аритмий сердца достоверно не отличалась от группы с аритмиями, что, вероятно, было обусловлено малым количеством больных в этой группе (значение двустороннего точного критерия Фишера находилось на уровне pf=0,146).
Анализ таблиц сопряженности параметров биоэлектрической активности головного мозга и аритмий сердца выявил наличие достоверной связи эпилептиформной активности с суправентрикулярными пароксизмальными тахикардиями (СВПТ) (С= 0,42; py=0,007), условно эпилептиформных феноменов с СВНТ (С= 0,34; py=0,025), дезорганизованного типа ЭЭГ с преобладанием тета-активности с ВСБ (С= 0,43; py=0,009).
Аналогичные результаты были получены и при использовании двустороннего точного критерия Фишера. При этом отмечалось достоверное преобладание частоты встречаемости СВПТ у больных с эпилептиформной активностью (pf=0,007), частоты встречаемости СВНТ у больных с условно эпилептиформными феноменами (pf=0,013) и частоты встречаемости ВСБ у больных с дезорганизованным типом ЭЭГ с преобладанием тета-активности (pf=0,011).
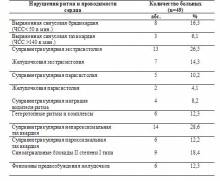
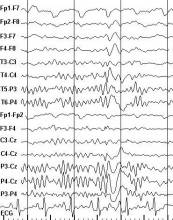
При синхронной записи ЭЭГ и ЭКГ нарушения сердечного ритма были зарегистрированы у 18 больных (36,7%), из них у 8 больных - СВЭ, у 6 больных - ЖЭ, у 3 больных - кратковременные (3-4 секунды) эпизоды синусовой тахикардии (СТ), возникающие одновременно с пароксизмальными вспышками на ЭЭГ, и у 1 больного - эпизоды СТ, возникающие за 1-2 секунды до появления пароксизмальных вспышек на ЭЭГ (рисунки 1 и 2). У 2 больных выявлялись СВЭ и СТ. Во время приступов СТ увеличение частоты сердечных сокращений (ЧСС) составляло от 12 до 26% и во всех случаях превышало 10 систол в минуту.
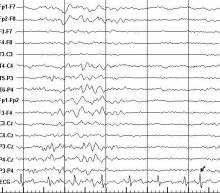
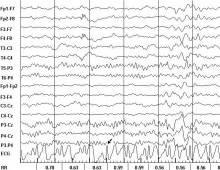
У 9 больных преждевременные сердечные сокращения имели характер спонтанных нарушений, а у 5 больных были отчетливо связаны с пароксизмальными вспышками на ЭЭГ, за которыми они следовали с временнóй задержкой, варьирующей в пределах от 1240 до 4330 мс (в среднем - 2900 ± 1044 мс) (рисунки 3 и 4).
Предшествовавшие возникновению экстрасистолии и СТ вспышки ЭЭГ-активности не обладали специфичностью и были, в основном, представлены генерализованными тета- и дельта-волнами. Лишь у одного больного они имели вид разрядов комплексов острая-медленная волна.
При спектральном анализе ЭЭГ у 6 из 9 больных со “спонтанной экстрасистолией” в период, соответствующий последнему предшествовавшему экстрасистоле кардиоинтервалу выявлялось увеличение мощности спектра медленных частот (1-5 Гц), составлявшее от 50 до 100% мощности спектра доминирующей частоты ритма ЭЭГ, а в ряде случаев даже превышавшее её.
Последние годы характеризуются повышенным интересом исследователей к проблеме цереброгенных аритмий сердца, включая изучение их связи с нарушениями функциональной активности церебральных структур на примере исследования биоэлектрической активности головного мозга. Большинство авторов сходятся в оценке высокой частоты встречаемости нарушений биоэлектрической активности головного мозга у больных с сердечными аритмиями и, в первую очередь, у больных с тахиаритмиями [11, 12].
В литературе рассматривается три концептуально возможных типа взаимоотношений тахиаритмий и нарушений биоэлектрической активности головного мозга: (1) пароксизмальная активность головного мозга нейрональным путем провоцирует изменения электрофизиологических свойств специализированной системы сердца и создает условия для инициализации пароксизмов тахиаритмии; (2) длительно существующие приступы тахиаритмий, нарушая церебральную гемодинамику, создают условия для формирования патологической активности головного мозга, которая в свою очередь провоцирует аритмии; (3) имеется единый биохимический механизм, приводящий к мембранным сдвигам в структурах мозга и сердца и обусловливающий пароксизмальную биоэлектрическую активность в обеих системах [12].
Результаты нашего исследования согласуются с данными других авторов [11-20, 22-24] и свидетельствуют о наличии тесной связи между нарушениями ритма и проводимости сердца и пароксизмальной активностью на ЭЭГ. Эта связь наиболее четко прослеживается в отношении суправентрикулярных тахикардий. При этом пароксизмальные суправентрикулярные тахикардии сочетаются с эпилептиформной активностью, а непароксизмальные суправентрикулярные тахикардии - с условно эпилептиформной активностью. Статистически достоверный характер связи, по нашему мнению, свидетельствует о наличии двух принципиально различных механизмов церебрального аритмогенеза. В первом случае роль пускового фактора играет эпилептический разряд с последующим вовлечением в синхронную эпилептическую активность церебральных вегетативных центров, а во втором случае первичная роль принадлежит дисфункции срединных структур мозга диэнцефального и верхнестволового уровня, обусловливающих как нарушения сердечного ритма, так и пароксизмальные вспышки высокоамплитудных волн на ЭЭГ. Из нейрофизиологии известно, что поражение структур ствола мозга на верхнем и среднем уровнях проявляется билатерально-синхронными медленными волнами в дельта- и тета-диапазонах и вспышками высокоамплитудных колебаний, а поражение гипоталамуса приводит к появлению на ЭЭГ билатерально-синхронных медленных колебаний чаще всего дельта диапазона [25]. Предположение о первичности дисфункции срединных структур по отношению к нарушениям сердечного ритма и пароксизмам на ЭЭГ объясняет кажущийся странным факт о нередком (до 76%) предшествовании нарушений сердечного ритма изменениям на ЭЭГ, выявленный в нашем исследовании и подтвержденный другими авторами [14, 15, 20]. В свете данного положения становится также ясным отсутствие жесткой детерминации и широкий разброс значений временных периодов возникновения экстрасистол после вспышек на ЭЭГ.
С наличием дисфункции диэнцефальных и стволовых структур, вероятно, связано и возникновение большинства других, помимо тахикардий, нарушений ритма и проводимости сердца у больных с заболеваниями головного мозга, о чем свидетельствуют увеличение мощности спектра медленных частот ЭЭГ перед экстрасистолами и достоверная связь возникновения брадикардий с увеличением медленной активности на ЭЭГ.
Выводы.
1. В возникновении цереброгенных аритмий сердца у больных с органической патологией головного мозга значительную роль играют пароксизмальные нарушения биоэлектрической активности церебральных структур.
2. Имеется два ведущих механизма церебрального аритмогенеза. В одном случае пусковым фактором является эпилептический разряд с вовлечением в синхронную эпилептическую активность церебральных вегетативных центров, а в другом первичная роль принадлежит дисфункции диэнцефальных и стволовых структур, обусловливающей нарушения сердечного ритма и пароксизмальные вспышки высокоамплитудных волн на ЭЭГ.
Литература.
1. Шпрах В.В., Синьков А.В., Синькова Г.М. и др. Цереброген-ные нарушения ритма и проводимости сердца у больных с последст-виями закрытой черепно-мозговой травмы. Невролог журнал; 2000: 5:1:31-34.
2. Oppenheimer S.M., Cechetto D.F., Hachinski V.C. Cerebrogenic cardiac arrhythmias. Cerebral electrocardiographic influences and their role in sudden death. Arch Neurol; 1990; 47:5:513-519.
3. Puerto S. Cerebrally induced cardiac arrhythmias (CICA). Heart Lung; 1994; 23:3:251-258.
4. Natelson B.H., Chang Q. Sudden death. A neurocardiologic phenomenon. Neurol Clin; 1993; 11:2:293-308.
5. Jallon P. Sudden death of epileptic patients. Presse Med; 1999; 28:11: 605-611.
6. Lathers C.M., Schraeder P.L. Review of autonomic dysfunction, cardiac arrhythmias, and epileptogenic activity. J Clin Pharmacol; 1987; 27:5:346-356.
7. Davis A.M., Natelson B.H. Brain-heart interactions. The neurocardiology of arrhythmia and sudden cardiac death. Tex Heart Inst J; 1993; 20:3:158-169.
8. Samuels M.A. Neurally induced cardiac damage. Definition of the problem. Neurol Clin; 1993; 11:2: 273-292.
9. Oppenheimer S.M. Neurogenic cardiac effects of cerebrovascular disease. Curr Opin Neurol; 1994; 7:1:20-24.
10. Hilz M.J., Dutsch M., Kolsch C. Epilepsy and autonomic diseases. Fortschr Neurol Psychiatr; 1999; 67:2:49-59.
11. Белоконь Н.А., Школьникова М.А., Белозеров Ю.М. и др. Хроническая непароксизмальная суправентрикулярная тахикардия у детей и подростков. Кардиология; 1990; 30:6:67-79.
12. Антюфьев В.Ф., Гузовский Е.В., Мякотных В.С. Характери-стика биоэлектрической активности структур головного мозга у паци-ентов с раз-личными видами тахиаритмий. Кардиология; 1992; 92:4:17-20.
13. Blumhardt L.D., Smith P.E., Owen L. Electrocardiographic accompaniments of temporal lobe epileptic seizures. Lancet; 1986; 1:8489:1051-1056.
14. Howell S.J., Blumhardt L.D. Cardiac asystole associated with epileptic seizures: a case report with simultaneous EEG and ECG. J Neurol Neurosurg Psychiatry; 1989; 52:6:795-798.
15. Keilson M.J., Hauser W.A., Magrill J.P. Electrocardiographic changes during electrographic seizures. Arch Neurol; 1989; 46:11:1169-1170.
16. Li L.M., Roche J., Sander J.W. Ictal ECG changes in temporal lobe epilepsy. Arq Neuropsiquiatr; 1995; 53:3-B:619-624.
17. Wilder Smith E., Wilder Smith A. Complex partial seizures as cause of transient cardiac arrhythmia. Schweiz Med Wochenschr; 1995; 125:46:2237-2243.
18. Massetani R., Strata G., Galli R., Gori S., Gneri C., Limbruno U., DiSanto D., Mariani M., Murri L. Alteration of cardiac function in patients with temporal lobe epilepsy: different roles of EEG-ECG monitoring and spectral analysis of RR variability. Epilepsia; 1997; 38:3:363-369.
19. Saussu F., van Rijckevorsel K., de Barsy T. Bradycardia: an unrecognized complication of some epileptic crises. Rev Neurol (Paris); 1998; 154:3;250-252.
20. Schernthaner C., Lindinger G., Potzelberger K., Zeiler K., Baumgartner C. Autonomic epilepsy--the influence of epileptic discharges on heart rate and rhythm. Wien Klin Wochenschr; 1999; 111:10:392-401.
21. Жирмунская Е.А. Клиническая электроэнцефалография. Об-зор литературы и перспективы использования метода. М 1991; 77.
22. Smith P.E., Howell S.J., Owen L., Blumhardt L.D. Profiles of instant heart rate during partial seizures. Electroencephalogr Clin Neurophysiol; 1989; 72:3:207-217.
23. Kiok M.C., Terrence C.F., Fromm G.H., Lavine S. Sinus arrest in epilepsy. Neurology; 1986; 36:1:115-116.
24. Kowalik A, Bauer J, Elger C.E. Asystolic seizures. Nervenarzt; 1998; 69:2:151-157.
25. Зенков Л.Р. Клиническая электроэнцефалография (с элемен-тами эпилептологии). Таганрог 1996; 358.
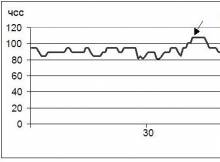
Рисунок 1. Фрагмент фоновой записи ЭЭГ и ЭКГ больной А. Диагноз: Опухоль (глиома) теменной и затылочной долей слева. Регистрируется эпизод синусовой тахикардии с ЧСС 107 в мин. (обозначено стрелкой), предшествующий генерализованной вспышке тета- и дельта-волн.
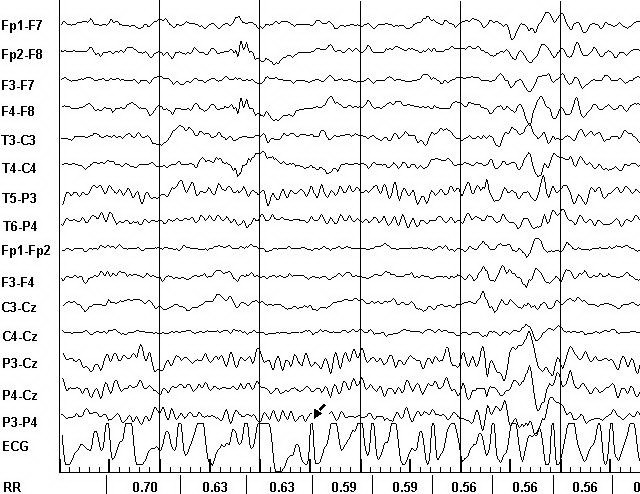
Рисунок 2. Фрагмент ритмограммы больной А. Стрелкой обозначено начало вспышки активности на ЭЭГ. Средняя ЧСС - 87 в мин., ЧСС во время вспышки - 107 в мин., увеличение ЧСС - 23%
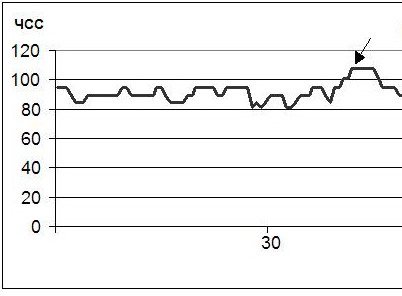
Рисунок 3. Фрагмент фоновой записи ЭЭГ и ЭКГ больного К. Диагноз: Парциальная симптоматическая (по-сттравматическая) эпилепсия с правосторонним очагом. Регистрируется суправентрикулярная экстрасистола (обозначена стрелкой), возникшая после генерализованной вспышки тета- и дельта-волн с задержкой 3480 мс.
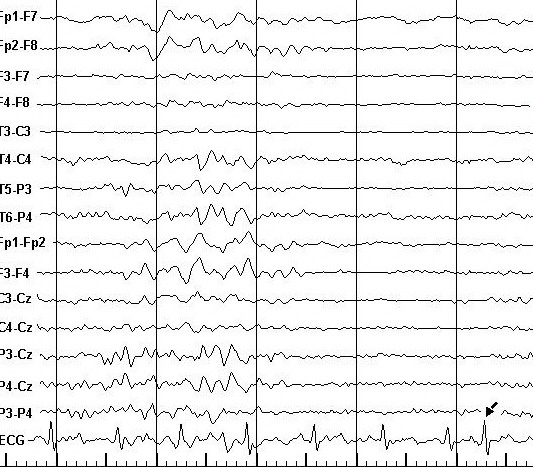
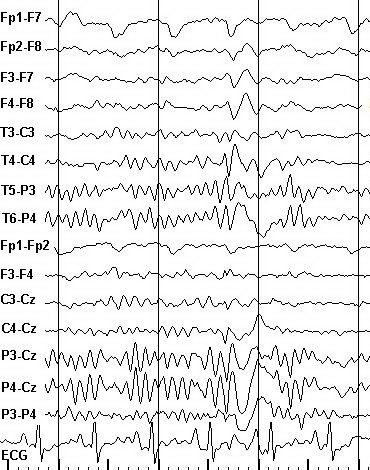
Рисунок 4. Фрагмент фоновой записи ЭЭГ и ЭКГ больного М. Диагноз: Генерализованная идиопатическая эпилепсия. Регистрируется суправентрикулярная экстрасистола (обозначена стрелкой), возникшая после генерализованного разряда комплексов острая-медленная волна с задержкой 1950 мс.
В 1 больнице Минска врачи впервые провели операции по профилактике образования тромбов
В 1–й минской клинической больнице врачи впервые провели серию вмешательств по профилактике образования тромбов, которые опасны для жизни. Оторвавшись и попав в кровеносное русло, они могут закупорить сосуд, в том числе головного мозга. Особенность в том, что на этот раз не пришлось задействовать хирургов и применять общий наркоз. А пять пациентов, мужчины и женщины средних лет, быстрее пошли на поправку. Больничные палаты они покинули буквально на второй–третий день.
Речь о новой эндоваскулярной, внутрисосудистой методике — окклюзии ушка левого предсердия (в этом месте чаще всего и образуется тромб). Она становится буквально спасением при нарушениях ритма сердца — трепетании предсердий и мерцательной аритмии. Изначально таким пациентам врачи назначают лекарства, разжижающие кровь. «Однако у определенного процента людей эффект от их применения низкий или недостаточный. Для некоторых эти средства и вовсе небезопасны, так как могут спровоцировать не только аллергические реакции, но и кровотечения, — рассказывает заведующий ангиографическим кабинетом 1–й клиники, главный внештатный рентгенэндоваскулярный хирург комитета по здравоохранению Мингорисполкома Павел Черноглаз. — Потому выход был один — операция. Но если раньше, работая на опережение, хирурги проводили либо сложное вмешательство со вскрытием грудной клетки, либо оперировали без скальпеля при помощи эндоскопа, то сегодня появилась альтернатива».
Смысл в том, что в верхней части бедра в области паха врач делает небольшой прокол, вводит в него медицинские инструменты и под контролем рентгена ведет их через бедренную, а после полую вену до самого левого предсердия. Сюда и доставляют так называемый зонтик, или окклюдер, который раскрывается и заполняет изнутри собой ушко. Готово — надежную «заглушку» поставили! Теперь у тромба нет шанса навредить. И на все про все — только 40 — 50 минут. Кстати, расходы по такому ювелирному вмешательству полностью берет на себя государство, хотя стоимость только спасительного зонтика — около 10 тысяч у.е.
Раньше столь высокотехнологичные вмешательства были исключительно прерогативой РНПЦ «Кардиология» и Республиканского клинического медицинского центра Управления делами Президента. Теперь по–новому спасать пациентов будут и городские больницы. В 1–й минской клинике прорывной технологией владеют уже четыре специалиста.
Справка «СБ»
Мерцательной аритмией, приводящей к инсульту, страдают около 200 тысяч жителей Беларуси.
Советская Белоруссия № 93 (24723). Среда, 20 мая 2015
Автор публикации: Алла МАРТИНКЕВИЧ

